Biomedical Applications of Mass Spectrometry: Organic Acidurias, Lipidomics and Natural Healings
Gerardo Manuel, Caballero (gerardomanuelcaballero@gmail.com)
Mariano Hernán, García (loboalbino@gmail.com)
Universidad Nacional Arturo Jauretche
Resumen
Se abordó el estudio de los ácidos grasos en muestras de plasma en el contexto del síndrome metabólico y de la hipertensión pulmonar arterial. Dichos compuestos juegan un rol significativo en el desarrollo de ambas patologías. Los resultados alcanzados son:
- el desarrollo y la puesta a punto del método de extracción de ácidos grasos totales de muestras de plasma humano y su transformación química en los correspondientes ésteres metílicos;
- el desarrollo y la definición del método de cromatografía de gases acoplada a espectrometría de masa para la determinación del perfil cualitativo de ésteres metílicos de ácidos grasos presentes en plasma;
- la caracterización estructural de los ácidos grasos encontrados en muestras de plasma de voluntarios sanos;
- la obtención de 99 muestras de pacientes con hipertensión arterial; y
- el comienzo del procesamiento de las muestras que tuvo que ser detenido por la cuarentena decretada con motivo de la pandemia de público
Por otro lado, el impacto generado por consecuencia del desarrollo del proyecto puede ser medido por los logros como la presentación de una comunicación en un congreso internacional de la European Respiratory Society, la publicación en el repositorio digital de la UNAJ de un libro de divulgación científica y la realización de dos charlas de divulgación (una sobre la tecnología empleada en el proyecto, la otra sobre la hipertensión pulmonar).
Palabras claves: acidemias, espectrometría, masa, HP, lípidos
Abstract
The project involved the study of fatty acids in plasma in the context of metabolic syndrome and arterial pulmonary hypertension. Those compounds play a significant role in the development of both pathologies. The results achieve are the following: 1) development of a complete protocol for plasmatic fatty acids extraction and chemical transformation into their corresponding methyl esters; 2) development of a gas chromatography – mass spectrometry protocol for the qualitative determination of plasmatic methyl esters fatty acids profile; 3) structural characterization of fatty acids found in healthy volunteer plasmas.
From other side, the impact generated as a consequence of the project development can be measured by the following achievements: 1) a communication to a European Respiratory Society Congress; 2) the publication of a book on the subject of scientific dissemination in UNAJ’s digital repository; 3) two dissemination talks, one about the technology employed in the project, the other related to pulmonary hypertension.
Keywords: Acidemias, Lipids, Mass, Spectrometry, PH
Introducción
El equipo de investigación constituido para el desarrollo de este proyecto había estado trabajando en el área de las aplicaciones biomédicas de la espectrometría de masa, en el marco de los proyectos oportunamente aprobados en las dos convocatorias previas UNAJ Investiga, y en el marco de colaboraciones con otras instituciones. Asimismo, parte de los integrantes del equipo contaban con muchos años de experiencia en espectrometría de masa. Por estos motivos, este proyecto apuntaba a aplicar, consolidar y desarrollar toda esa experiencia previa en cuatro problemas concretos factibles de estudiar con la tecnología mencionada:
- la puesta a punto final de la metodología analítica de análisis de ácidos orgánicos en orina de neonatos;
- el desarrollo de un método de análisis cualicuantitativo de ácidos grasos en plasma para su aplicación posterior en el estudio del perfil lipídico de pacientes diagnosticados con síndrome metabólico (SM) y pacientes de grupo control;
- estudio del perfil cualicuantitativo de esteroles libres y totales en muestras de plasma de los grupos mencionados en el punto anterior;
- la determinación de la composición química de las oleorresinas obtenidas de las bayas de aguaribay (Schinus molle L.) como apoyo a la aplicación de estas oleorresinas en productos cicatrizantes.
Posteriormente, dada la capacidad adquirida durante los trabajos relacionados al segundo problema, así como la vinculación establecida con la Unidad de Neumonología del Hospital El Cruce (HEC), se sumó un quinto objetivo: el estudio del perfil de ácidos grasos de pacientes con hipertensión pulmonar arterial (HPA).
¿Cuáles son los antecedentes en estas áreas diversas y por qué la espectrometría de masa? La espectrometría de masa es una técnica analítica nacida a principios del siglo XX que se ha consolidado en diversas áreas biomédicas desde 1990, en particular acoplada a la cromatografía de gases (GC-MS, por su sigla en inglés) o de líquidos (LC-MS, también por su sigla en inglés). Estas técnicas ofrecen un mayor nivel de sensibilidad y especificidad para muchos analitos comparadas con otras técnicas usuales en los laboratorios de análisis clínicos (Garg y Hammett-Stabler, 2010), como así también en las nuevas áreas de la metabolómica y la lipidómica (Quehenberger et al., 2010). Es de destacar que, al momento de iniciar este proyecto, este grupo de investigación se encontraba trabajando en el Laboratorio N° 1 del Centro de Medicina Traslacional (CEMET) del HEC con un instrumento de LC-MS, y otro de GC-MS a disposición para el desarrollo de sus tareas de investigación. El primer instrumento había sido comprado por el HEC con el asesoramiento del director de este proyecto, quien también se encargó de gestionar, junto al doctor Arnaldo Medina, la donación del segundo instrumento mencionado, desde la entonces Secretaría de Deporte de la Nación al HEC. Luego, este equipo de investigación se ocupó de todo lo relacionado con la reparación y puesta a punto del instrumento de GC-MS, así como de su traslado e instalación en el laboratorio mencionado.
Uno de los campos donde las técnicas de GC-MS son sumamente útiles es el análisis de ácidos orgánicos en orina, fluido que contiene cientos de ácidos orgánicos diferentes provenientes de diversas fuentes, cuya variedad y concentración puede modificarse en un metabolismo anormal. Por ello, estos ácidos orgánicos excretados en orina sirven como indicadores de diversos trastornos metabólicos que pueden presentarse en neonatos; en consecuencia, el análisis de estos compuestos es de vital importancia para una detección rápida de dichos trastornos. El pronto tratamiento de estas anomalías congénitas puede evitar el desarrollo de retardo mental, e incluso la muerte de bebés recién nacidos. Debido a esto, este análisis es esencial en el estudio de muestras de orina de neonatos sospechados de padecer un error congénito del metabolismo de los ácidos orgánicos (Jones y Bennett, 2010). Cuando un trastorno de este tipo se presenta, el resultado suele ser la excreción de cantidades anormales de un metabolito normal en orina o la aparición de metabolitos anormales (Pasquali y Sawyer, 2008), y estas anomalías pueden ser rápidamente detectadas mediante técnicas de GC-MS.
En este campo, y en relación al primer objetivo, parte de este grupo de investigación había estado trabajando en las instalaciones del Laboratorio de Control de Doping del Centro Nacional de Alto Rendimiento Deportivo (CeNARD), la misma institución que donó el equipo de GC-MS al HEC, gracias a la colaboración del director de dicho laboratorio, y en el marco de la primera convocatoria UNAJ Investiga. Allí se consiguió poner a punto un método de análisis de ácidos orgánicos en orina significativamente ventajoso respecto a los métodos internacionales de uso corriente en ese momento (Jones y Bennett, 2010), en cuanto al tiempo y la sencillez en la preparación de la muestra, así como en la duración del análisis cromatográfico. Como estos resultados alentadores fueron conseguidos empleando un instrumento de GC-MS con tecnología de trampa de iones, el método debía ser adecuadamente transferido al instrumento de GC-MS con tecnología de cuadrupolo, con el que el grupo contaba en el Laboratorio N° 1 mencionado. Se apuntaba en ese momento a la culminación de la puesta a punto del método, para una posterior eventual transferencia a algún laboratorio de análisis clínico del ámbito público; en un verdadero ejemplo de medicina traslacional, ya que modificaciones de química analítica básica redundarían por transferencia inmediata de estos conocimientos en un mejor servicio médico para la detección de enfermedades congénitas raras.
En el caso del segundo objetivo, al momento de iniciar el proyecto, el equipo de investigación estaba trabajando en conjunto con el doctor Carlos Pirola, cuyo grupo del Instituto de Investigacines Médicas “Alfredo Lanari” posee experiencia en SM. Este síndrome es una entidad clínica altamente prevalente, que está caracterizado por una combinación de diversos factores de riesgo (diabetes tipo 2, dislipidemias, obesidad central, hipertensión arterial, y otros fenotipos tales como enfermedad grasa del hígado de etiología no alcohólica) para un desenlace común: la enfermedad cardiovascular (Sookoian y Pirola, 2008).
Una de las características más significativas del SM es el desarrollo de la insulinorresistencia (IR) (Sookoian y Pirola, 2012), pero como toda enfermedad compleja, tiene su causa en múltiples factores ambientales y genéticos. De los factores de riesgo mencionados, la dislipidemia puede diagnosticarse mediante análisis de rutina de los niveles de colesterol y triglicéridos. Sin embargo, el creciente número de personas con enfermedades metabólicas demanda un análisis más detallado de los lípidos, tanto para propósitos de diagnóstico como para control de la eficacia de tratamientos terapéuticos. Dentro del conjunto de lípidos se encuentran los ácidos grasos, sustancias que están, por un lado, en lípidos complejos y, por otro, libres en la circulación. Estos últimos provienen de diversas fuentes: dieta, liberación desde tejido adiposo, biosíntesis. Se sabe que los niveles y el perfil de ácidos grasos plasmáticos están relacionados a ciertos factores de riesgo asociados al SM. Por ejemplo, la mayoría de las personas obesas tienen altos niveles plasmáticos de ácidos grasos libres, debido a una mayor liberación desde el tejido adiposo expandido. El aumento a largo plazo en los niveles plasmáticos de ácidos grasos libres finalmente inhibe la acción antilipolítica de la insulina, lo cual incrementa más aún la velocidad de liberación de ácidos grasos a la circulación, y contribuye al desarrollo de resistencia a la insulina y a diabetes de tipo 2 (Boden, 2006).
Sin embargo, no todos los tipos de ácidos grasos contribuyen igualmente a la alteración sistémica de la acción de la insulina, ya que la grasa rica en ácidos grasos saturados promueve resistencia a la insulina, pero los ácidos grasos monoinsaturados y poliinsaturados la reducen (Riccardi, Giacco y Rivellese, 2004). Con estos antecedentes, se había propuesto el estudio del perfil cualicuantitativo de ácidos grasos libres y totales en muestras de plasma, por un lado, de personas del grupo con factores de riesgo y, por el otro, de personas del grupo control. En ambos casos se hizo mediante técnicas de GC-MS y se organizó el perfil global en las subclases de ácidos grasos saturados, monoinsaturados, y poliinsaturados; con la hipótesis de que los distintos fenotipos del SM presentarían perfiles lipídicos diferentes. En el presente proyecto se proponía la culminación del desarrollo de la metodología de análisis de ácidos grasos totales y libres en muestras de plasma, ajustando todos los parámetros del método de GC-MS y resolviendo ciertos detalles experimentales del proceso de derivatización y extracción de los ácidos grasos totales y libres del plasma, como también la puesta a punto del método de cuantificación de ácidos grasos.
En relación al tercer objetivo, el foco estaba puesto en la categoría de lípidos esteroles donde se encuentra el colesterol, el más abundante de los esteroles plasmáticos que existe tanto libre como esterificado con ácidos grasos; habiéndose encontrado en plasma más de veintidós especies diferentes de ésteres de colesterol (Quehenberger et ál, 2010). El plasma humano contiene también campesterol y sitosterol, los cuales no son sintetizados en humanos, sino que provienen enteramente de la dieta de origen vegetal. En personas normales, estos esteroles vegetales están presentes solo en pequeñas cantidades, siendo el colesterol más del 99% de todos los esteroles circulantes, pero en la sitosterolemia los niveles en plasma de esteroles vegetales están marcadamente elevados. En estos casos se hace necesario un panel completo de esteroles plasmáticos para determinar un diagnóstico diferencial y seleccionar el mejor tratamiento. Otro esterol de relevancia terapéutica presente en el plasma normal es el latosterol, precursor biosintético del colesterol. El latosterol puede tener valor diagnóstico como indicador de la síntesis corporal de colesterol (Björkhem et al., 1987), ya que este esterol no proviene de la dieta. En este caso el objetivo planteado era el estudio del perfil cualicuantitativo de esteroles libres y totales en muestras de plasma de pacientes con SM y del grupo control, mediante técnicas de GC-MS. Los datos globales del grupo control permitirían tener valores de referencia de población sana del Área Metropolitana de Buenos Aires y se evaluaría la posibilidad de que el perfil de esteroles, en particular la concentración del latosterol, permitiera discriminar entre individuos de ambos grupos.
Como una extensión del segundo objetivo, aprovechando la experiencia adquirida en su desarrollo, y en colaboración directa con la Unidad de Neumonología del HEC, se planteó naturalmente la propuesta de establecer una metodología analítica robusta basada en GC-MS para la caracterización y cuantificación de ácidos grasos en plasma de pacientes con salud y de pacientes diagnosticados con HPA. ¿Por qué estudiar los ácidos grasos en el contexto de esta enfermedad? La HPA es una enfermedad compleja multifactorial caracterizada por un aumento en la resistencia vascular pulmonaria y por procesos de remodelación vascular, que conducen a la disfunción del ventrículo derecho (DVD). Existe numerosa evidencia de que la DVD observada en la HPA puede estar asociada con algunos componentes del SM, como por ejemplo la resistencia a la insulina (Talati y Hemnes, 2015). La relación entre la DVD y los metabolitos de ácidos grasos/glucosa en la HPA está caracterizada por un corrimiento en la utilización de fuentes de energía hacia un incremento en la utilización de glucosa y una disminución del consumo de ácidos grasos. La DVD puede estar causada por un metabolismo de ácidos grasos mal adaptado, que resulta de un incremento en la absorción de estos y un desbalance entre la oxidación de ácidos grasos y glucosa en las mitocondrias. Existe también una relación probada entre los ácidos grasos y los procesos inflamatorios, donde las mitocondrias juegan un rol central (Ross et al., 2015). Por estas razones, las investigaciones en lípidos, y en particular en ácidos grasos, asociados a la HPA podrían abrir un abanico de posibilidades en diferentes niveles. No solo permitirían una aproximación a una explicación profunda de los procesos fisiológicos relacionados al desarrollo y a la evolución de la HPA, sino que también podrían ser la herramienta para el descubrimiento de metabolitos claves de la patogenia. Estos metabolitos funcionarían como biomarcadores de diagnóstico y seguimiento, brindando una evaluación más precisa del tratamiento y prognosis de la patología.
El cuarto, y último, objetivo surgió como una extensión de la colaboración iniciada en 2014 con el grupo de la doctora Lucía Pollio del Departamento de Ciencia y Tecnología de la Universidad Nacional de Quilmes (UNQ). En ese momento, el director de este proyecto ayudó a establecer la composición química de las oleorresinas obtenidas de bayas de aguaribay (Schinus molle L.), determinando que estaban compuestas principalmente por hidrocarburos terpénicos y sesquiterpénicos, así como también por alcoholes sesquiterpénicos (Padin, 2015). El grupo de la doctora Pollio había encontrado previamente actividad antibacteriana en estas oleorresinas y, posteriormente, reconoció sus propiedades antioxidantes y cicatrizantes (Caballero, Padin y Pollio, 2014), como así también ciertas propiedades antimicrobianas sobre hongos y levaduras (Padin, Caballero y Pollio, 2015). El grupo de investigación de la UNQ asociado se había planteado estudiar en profundidad la capacidad cicatrizante de estas oleorresinas, además del diseño y de la caracterización de nanopartículas lipídicas sólidas como vehículos para estos extractos con el fin de obtener cremas con propiedades antimicrobianas y cicatrizantes. En soporte a estas investigaciones, este equipo se propuso estudiar más en detalle la composición química de las oleorresinas mediante GC-MS, ya que el trabajo previo en colaboración mencionado había demostrado que la composición química precisa de las oleorresinas influye en la actividad antimicrobiana, y esta composición puede variar según el momento de recolección de las bayas.
Adicionalmente, dada la vinculación del director de este proyecto con la UNQ y su natural relación con varios de sus investigadores, hacia mediados de 2019 se estableció otra colaboración, en este caso con la doctora Nadia Chiaramoni y el doctor Mariano Grasselli del Departamento de Ciencia y Tecnología de la universidad mencionada, para la confirmación estructural mediante LC-MS de un péptido sintético y sus productos de reacción química. Este péptido, diseñado y sintetizado en el Laboratorio de Microbiología Molecular de la UNQ, presenta carga positiva y es capaz de generar poros en membranas bacterianas (Faccone, Veliz, Corso et al., 2014). El extremo N-terminal de este péptido es un residuo de serina, que puede ser oxidado con periodato de sodio. Esta reacción se ensayó siguiendo protocolos de literatura (Geoghegan y Stroh, 1992) con el objetivo de obtener un péptido modificado con un grupo aldehído (estrictamente un grupo α-N-glioxililo) en su extremo N- terminal. El péptido así modificado puede posteriormente usarse como sonda de prueba de reacciones de conjugación con un exceso del reactivo dihidrazida del ácido adípico, el cual forma enlaces hidrazona con el grupo aldehído, derivando en otro péptido modificado portador este de un grupo alquilhidrazida. Estos ensayos apuntan a adherir esta modificación a una nanopartícula proteica, hecha con albúmina de suero bovino (BSA), para incrementar la concentración local del péptido en el sitio de infección.
Metodología
En el caso del primer objetivo, para trasladar el método desarrollado en el CeNARD al instrumento del CEMET, se pensó en el desarrollo de un procedimiento que utilizara el modo de funcionamiento de monitoreo selectivo de iones (SIM, por su sigla en inglés) del analizador de cuadrupolo disponible en el instrumento de GC-MS del CEMET. Para esto, de los espectros de masa de los patrones de ácidos orgánicos disponibles se seleccionaron dos iones significativos (el ion molecular y el pico base) para incluirlos en las ventanas de tiempos de retención correspondientes a cada uno de los ácidos orgánicos bajo estudio. De esta manera, se podría conseguir la impresión de un reporte conformado por dos ventanas para cada ácido orgánico a investigar, en cuyo centro exacto aparecerían las señales investigadas. Cada página de este reporte estaría conformada por nueve conjuntos de ventanas (dos para cada compuesto como se mencionó) que serían de muy sencilla inspección, ya que, por comparación con el reporte correspondiente a una orina normal, una anomalía sería rápidamente detectada por la observación de dos señales muy intensas en el centro de la ventana correspondiente al ácido orgánico cuya concentración se encuentra patológicamente elevada, o bien ha desaparecido. De acuerdo a lo descripto, un informe de cuatro páginas podría incluir a los 36 ácidos orgánicos más comúnmente asociados a los trastornos congénitos del metabolismo de neonatos, y por esto la inspección de un lote de treinta muestras que un laboratorio puede procesar en un día normal de trabajo podría realizarse en aproximadamente una hora después de concluidos los análisis por GC-MS.
En el desarrollo del segundo objetivo, se debía terminar de definir el procedimiento químico de extracción y derivatización de ácidos grasos ligados a lípidos complejos, y ácidos grasos libres en circulación en muestras de plasma, transformándolos en sus correspondientes ésteres metílicos. Para realizar la extracción y derivatización mediante una reacción de transesterificación de aquellos ácidos grasos ligados a lípidos complejos, hemos realizado diversas pruebas teniendo en cuenta la metodología que se describe en la literatura. Hemos modificado en varios aspectos la metodología de un trabajo en particular, que era el que más se adaptaba a la tecnología y los recursos de este equipo de trabajo (Rodríguez-Ruiz, Belarbi, García Sánchez y López Alonso, 1998). En primer lugar, se preparan las soluciones de los ácidos grasos a utilizar como estándar interno. Para esto, se disuelven 25,0 mg de ácido tridecanoico (C13:0) y 25,0 mg de ácido tricosanoico (C23:0) en 1 ml de metanol/tolueno (3:2 v/v).[1] Luego, a 100 microlitros de plasma se agregan 5 microlitros de la solución de estándares, 1 ml de la solución de metilación (metanol/cloruro de acetilo, 20:1 v/v) y 0,5 ml de hexano. La mezcla se calienta en bloque calefactor a 100 °C durante 60 minutos. Después de dejar enfriar hasta temperatura ambiente, se agrega 1 ml de agua destilada, se centrifuga durante 15 minutos a 2000 g, y de la fase superior (solución en hexano) se toman 100 microlitros que se transfieren a un vial de inyección para GC. Este protocolo permite preparar los ésteres metílicos del total de ácidos grasos: los libres en circulación y los ligados a lípidos complejos. Por su parte, la modificación del tiempo y la temperatura de la reacción de derivatización (45 minutos a 25 °C) permite esterificar solamente los ácidos grasos libres (Lepage y Roy, 1988). En este caso, la reacción de metilación debe cortarse mediante el agregado cuidadoso de 3 ml de una solución de carbonato de potasio al 6%. Luego se agregan 150 microlitros de hexano, la mezcla se agita y se centrifuga durante 10 minutos a 2000 g, y de la fase superior se toman 50 microlitros que se transfieren a un vial de inyección para GC.
Con el propósito de establecer las condiciones cromatográficas y de espectrometría de masa óptimas para el análisis de los extractos obtenidos como se describió arriba, se trabajó inicialmente con una mezcla comercial de patrones de 37 ésteres metílicos de ácidos grasos saturados e insaturados, los de mayor importancia y cantidad en el organismo, de C4 hasta C24 (Supelco FAME Mix). Esta mezcla se analizó con el instrumento de GC-MS marca Hewlett Packard (cromatógrafo de gases 5890, serie II-Plus, espectrómetro de masa 5972) equipado con una columna de cromatografía de gases de fase estacionaria polar, cianopropilo de bajo sangrado (VF-23ms), de 30 m de longitud x 0,25 mm de diámetro interno x 0,25 µm de espesor de fase. Este instrumento utiliza el programa Enhanced ChemStation G1701BA, versión 01.00 para la adquisición, la visualización y el procesamiento de datos.
A continuación, las condiciones de operación del cromatógrafo de gases y del espectrómetro de masa puestas a punto para el análisis de los patrones de ésteres metílicos de ácidos grasos, y para los primeros ensayos con muestras de plasma de voluntarios sanos:
- Inyector del cromatógrafo
- Temperatura: 250 °C; volumen de inyección: 2,0 microlitros; presión de cabeza: 10 psi; modo de inyección: venteo (split); relación de venteo: 10:1.
- Horno del cromatógrafo
- Temperatura inicial: 50 °C; tiempo inicial: 7,0 minutos; rampa de temperatura 1: 10 °C/minuto; temperatura intermedia: 150 °C; rampa de temperatura 2: 1 °C/minuto.
- Temperatura final: 195 °C; tiempo final: 3 minutos; tiempo total: 65 minutos.
- Interfase
- Temperatura: 300 °C.
- Espectrómetro de masa
- Temperatura de la fuente de iones: 170 °C; energía de ionización: 70 eV voltaje del repulsor: 20 V; modo de operación del cuadrupolo: barrido (scan) rango de m/z barrido: 40-400; velocidad de barrido: 2,11 barridos/segundo.
- Intervalo de adquisición de datos: 4-65 minutos; voltaje del electromultiplicador: 1600 V
El desarrollo ulterior del método implicó algunos cambios en los parámetros precedentes:
- Inyector del cromatógrafo
- Relación de venteo: 5:1.
- Horno del cromatógrafo
- Temperatura inicial: 50 °C; tiempo inicial: 7,0 minutos; rampa de temperatura 1: 10 °C/minuto; temperatura intermedia 1: 150 °C; rampa de temperatura 2: 1,5 °C/minuto.
- Temperatura intermedia 2: 175 °C; rampa de temperatura 3: 2 °C/minuto temperatura final: 195 °C; tiempo final: 8,3 minutos; tiempo total: 52 minutos.
- Espectrómetro de masa
- Intervalo de adquisición de datos: 4-52 minutos; voltaje del electromultiplicador: 2100 V.
Los métodos de preparación de muestras y de análisis por GC-MS, desarrollados según lo indicado, se aplicaron luego al análisis de muestras de plasmas de voluntarios sanos para ajustar los detalles de todo el procedimiento analítico, y para conseguir información preliminar sobre el patrón de ácidos grasos esperable de encontrar al momento de analizar las muestras destinadas al desarrollo del segundo objetivo del proyecto y del subproyecto vinculado a la HPA. En estas muestras, la cuantificación de los ésteres metílicos de ácidos grasos se realiza aplicando la fórmula: CA = [área de analito/área de estándar interno] x CEI (donde CA: concentración del analito; y CEI: concentración del estándar interno más cercano en tiempo de retención al analito correspondiente); de esta manera se obtienen resultados semicuantitativos. Con los valores individuales de concentración obtenidos se podrán calcular los promedios y las desviaciones estándar. Adicionalmente, los datos individuales serán analizados en el entorno de programación R, aplicando distintos test estadísticos multivariantes, como por ejemplo PCA y PLS-DA. Como se mencionó, los resultados obtenidos por el método de cuantificación señalado son semicuantitativos; sin embargo, por diversos motivos, no se considera necesaria una cuantificación rigurosa de cada analito individual. El principal motivo es que solo se buscan diferencias significativas entre los grupos de pacientes; por ello, la aplicación del mismo método de cuantificación a todas las muestras (población control y población diagnosticada con SM o HPA) asegura que el posterior tratamiento estadístico de los valores obtenidos brinde resultados confiables sin sesgo. Además, una cuantificación rigurosa demandaría la compra de patrones marcados isotópicamente de cada uno de los ácidos grasos de interés. Esto resulta muy dificultoso dado el altísimo costo en dólares de dichos patrones y la imposibilidad de conseguir algunos de ellos en el mercado.
En relación al objetivo de la HPA, durante los últimos meses del desarrollo de este proyecto, investigadores asociados al grupo de Neumonología del HEC habían conseguido recolectar unas 99 muestras de sangre de los pacientes, con consentimiento informado para participar del proyecto, pertenecientes al grupo control y al grupo de diagnosticados con HPA. Esas muestras, más las muestras de plasma correspondientes, se encuentran adecuadamente resguardadas en freezers de -80 °C ubicados en el segundo piso del CEMET.
Los péptidos tanto naturales como sintéticos, al igual que sus productos de transformación química, pueden caracterizarse rápidamente por LC-MS utilizando una fuente de electroespray como la que posee el instrumento instalado en el CEMET. Cuando se trabaja con mezclas es necesaria una purificación previa utilizando el cromatógrafo de líquidos acoplado al espectrómetro de masa. En el caso de la colaboración con la UNQ en este tema, eso no fue necesario por tratarse de productos previamente purificados. Por ello, tanto el péptido sintético como sus productos de reacción fueron infundidos directamente a la fuente de electroespray mediante la bomba de infusión con la que cuenta el instrumento mencionado. Las tareas relacionadas a la síntesis del péptido sintético y a su transformación química fueron desarrolladas en laboratorios de la UNQ. Este grupo se encargó del análisis de dichos productos, preparados en solución de 0,05% de ácido fórmico en agua (concentración del orden de 20 microgramos/microlitro en el caso del péptido sintético y de 20 micromolar en el caso de los productos de reacción), mediante infusión directa de las soluciones al instrumento de triple cuadrupolo TSQ Quantum Access Max provisto de fuente de electroespray (H-ESI II). Así, los principales parámetros instrumentales usados para los análisis mencionados:
- Velocidad de infusión:
- 5 microlitros/minuto (jeringa de 500 microlitros).
- Fuente de electroespray:
- Voltaje del electrodo: 3500 V; temperatura del capilar: 270 °C; presión gas vaina (nitrógeno): 5 psi; voltaje del cono colador (offset): -5 V.
- Analizador de masas:
- Analizador empleado: Q1.
- Modo de barrido: barrido completo (full scan); rango de barrido (m/z): 200-1000.
- Tiempo de barrido: 1 s.
Resultados
Durante el desarrollo del proyecto se encontraron una serie de dificultades técnicas y humanas que retrasaron su avance e impidieron la concreción de varios de sus objetivos. Estas dificultades se describen con detalle en el Anexo I; acá solo es necesario mencionar una serie de fallas en el módulo del cromatógrafo del instrumento de GC-MS, un instrumento de la década del 90 reacondicionado y puesto operativo nuevamente en el año 2015 que, como todo instrumento de estas características, suele tener fallas recurrentes, frecuentes en particular cuando se carece de un contrato de mantenimiento preventivo anual como fue el caso. Un segundo y muy serio problema fue una falla general del programa de control operativo del instrumento que impedía el normal desarrollo de una secuencia de inyección. Todos los contratiempos con los programas y el hardware del instrumento de GC-MS retrasaron más de seis meses el desarrollo de los otros objetivos del proyecto.
En cuanto a los resultados concretos, durante el desarrollo del proyecto se terminaron de definir las condiciones precisas del método GC-MS para la determinación cualicuantitativa de ácidos grasos en muestras de plasma. También se puso a punto la técnica de preparación de la muestra para extraer y derivatizar los ácidos grasos plasmáticos. Se presenta abajo, en la Figura 1, el cromatograma de corriente iónica total (TIC, por su sigla en inglés) de una mezcla de patrones de ésteres metílicos obtenido con las primeras condiciones instrumentales indicadas en la sección “Metodología”. Es pertinente aclarar que los análisis por GC-MS de mezclas de compuestos brindan como resultado un cromatograma (denominado “cromatograma total de iones” o “cromatograma TIC”), el cual es un gráfico de abundancia de la corriente de iones en función del tiempo y en el que se encuentra la información del tiempo de retención de cada uno de los componentes de la mezcla, así como los correspondientes espectros de masa de ionización electrónica. Estos espectros pueden ser usados para la asignación de la estructura química en el caso de un compuesto desconocido o para su verificación de en el caso de compuestos conocidos. El proceso de asignación estructural puede ser asistido mediante la búsqueda en bases de datos de espectros de masa (biblioteca de espectros, o “espectrotecas” según el neologismo usado en la jerga de la espectrometría de masa), pero la palabra final está muchísimas veces en la inspección manual de los espectros realizada por el operador experto.
Un segundo resultado obtenido fue la puesta a punto de la metodología de extracción y transformación del total de ácidos grasos en plasma, los ligados a lípidos complejos y los libres en circulación, en sus correspondientes ésteres metílicos, según lo detallado en la sección “Metodología”. Estos extractos fueron analizados inicialmente con el mismo protocolo instrumental que el indicado para la obtención del perfil de patrones de ésteres metílicos presentado en la Figura 1, utilizando en los primeros ensayos concentraciones no ajustadas de los estándares internos (ácido tridecanoico, C13:0, y ácido tricosanoico, C23:0). Se presenta, en la Figura 2, el cromatograma TIC de los ésteres metílicos de ácidos grasos presentes en plasma de un voluntario sano. Como se observa, el pico correspondiente a C13:0 aparece como el más intenso del cromatograma (tiempo de retención = 17,65 min.), mientras que el pico del otro estándar (C23:0), a tiempo de retención 38,04, es de muy baja intensidad.
Figura 1
Cromatograma TIC de la mezcla de patrones de ésteres metílicos de ácidos grasos
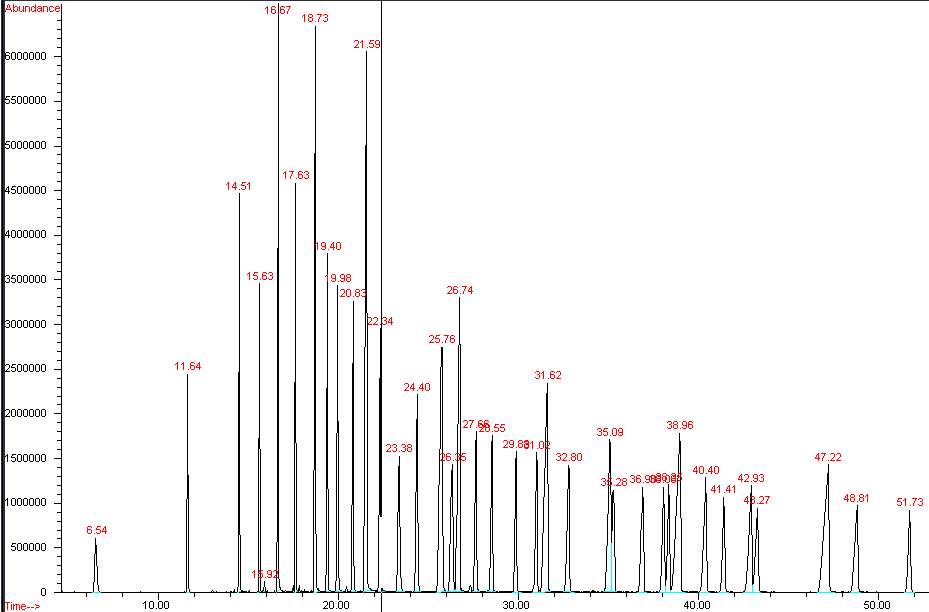
Figura 2
Cromatograma total de iones (TIC) de ésteres metílicos de ácidos grasos en plasma con C13:0 (tr. 17,65) y C23:0 (tr. 38,04 min) como estándares internos
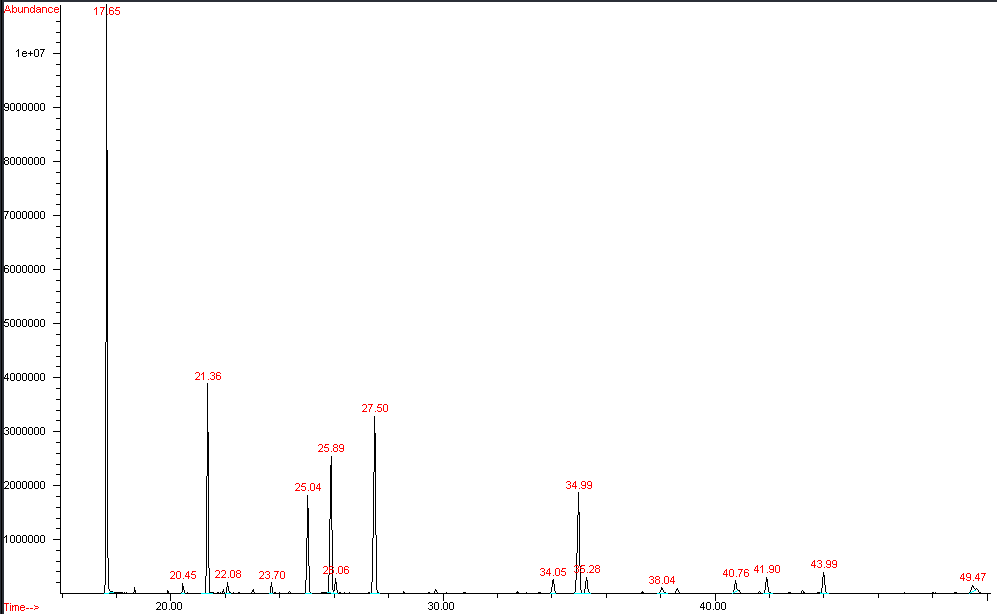
Disminuyendo la concentración del ácido tridecanoico, aumentando la concentración del segundo estándar interno, el ácido tricosanoico, y luego aplicando el segundo protocolo instrumental indicado en la sección de metodología, se obtuvieron mejores resultados en cuanto a la relación de áreas estándar interno/ácido graso, parámetro significativo para una cuantificación relativa más precisa. En la Figura 3 se presenta el cromatograma TIC así obtenido donde pueden observarse los picos de ambos estándares internos a 17,7 y 38,4 minutos, los que se utilizan para la cuantificación de los ésteres metílicos de ácidos grasos que eluyen en el rango 10-30 minutos y 30-50 minutos respectivamente. Mediante estos protocolos analíticos, y por comparación de tiempos de retención e inspección manual de los correspondientes espectros de masa, se estableció la presencia, en muestras de plasma de voluntarios sanos, de los ácidos grasos indicados en la Tabla 1, cada uno de ellos en forma de sus ésteres metílicos.
Figura 3
Cromatograma total de iones (TIC) de ésteres metílicos de ácidos grasos en plasma con C13:0 (tr 17,7 min) y C23:0 (tr 38,4 min) como estándares internos
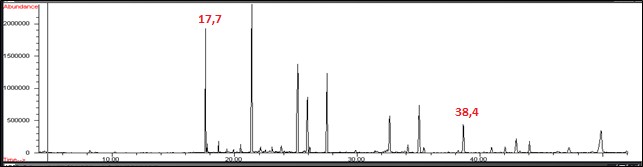
Los resultados obtenidos son muy alentadores. Como puede observarse en los cromatogramas y en la Tabla 1, han sido identificados positivamente, y adecuadamente separados por cromatografía, veintiún ácidos grasos provenientes de plasma de voluntarios sanos pertenecientes a las tres familias en las que suelen agruparse estos compuestos: saturados, monoinsaturados y poliinsaturados. Dado lo observado, la integración de las señales para determinar el área de cada pico y el posterior cálculo de las concentraciones en plasma de cada uno de estos ácidos grasos será de sencilla concreción. Debido al protocolo de preparación de muestras empleado, estos ácidos grasos corresponden al conjunto total de ácidos grasos: ligados a lípidos complejos y libre en circulación.
En el caso de la colaboración con la UNQ, en la caracterización estructural de un péptido sintético y de sus productos de reacción química, se consiguió la verificación de la estructura del péptido sintético preparado en un equipo de síntesis automática de péptidos perteneciente a la UNQ. En efecto, como se observa en la Figura 4, del espectro de electroespray del péptido sintético se puede calcular que su peso molecular es 2442,5 g/mol, valor coincidente con el peso molecular teórico que surge de la secuencia de aminoácidos preparada. Sin embargo, los análisis de los espectros de electroespray del producto de oxidación del péptido sintético y del subsecuente producto de reacción con la hidrazida mencionada dieron resultados confusos que sugieren que la reacción de formación del aldehído se consiguió parcialmente, pero el producto obtenido no estaba adecuadamente purificado.
Tabla 1
Ésteres metílicos de ácidos grasos en muestras de plasma
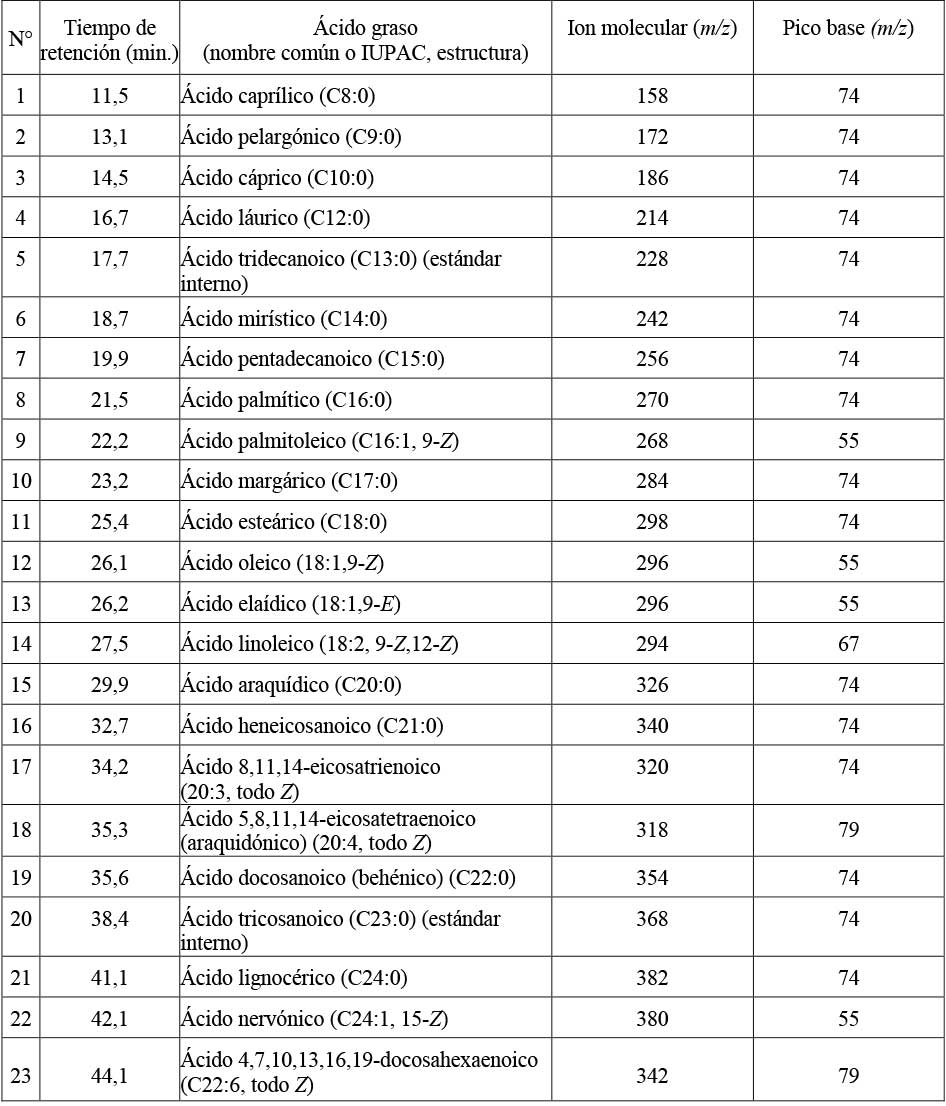
Figura 4
Espectro de electroespray del péptido sintético de peso molecular 2.442,5 g/mol.
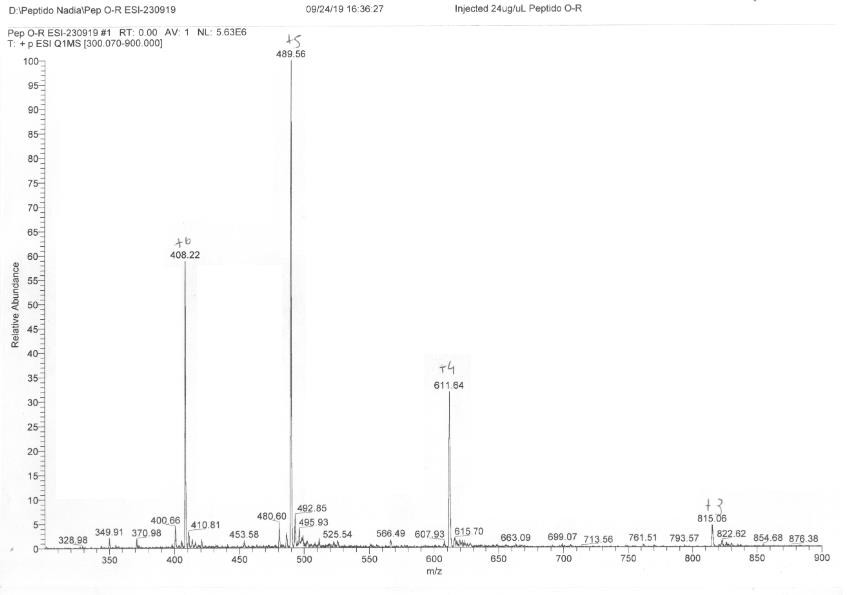
Nota. Se indican las cargas de los iones a partir de los cuales se calcula el peso molecular.
Discusión
Los resultados obtenidos son muy alentadores en relación a la concreción del objetivo final de cuantificar el conjunto de ácidos grasos totales, tanto libres en circulación como ligados a lípidos complejos, presentes en muestras de plasma de pacientes diagnosticados con hipertensión pulmonar y de voluntarios sanos del grupo control, y el ulterior análisis estadístico de los resultados cuantitativos obtenidos. Esto es así ya que, con toda la experiencia adquirida, las tareas restantes que corresponden al ensayo de extracción de ácidos grasos libres en circulación en plasma, el análisis de esos extractos por GC-MS, y el ajuste de los parámetros de integración de las señales cromatográficas, serían factibles de completar en un breve período. Luego, el método completo así desarrollado podría ser aplicado al conjunto de muestras de plasma almacenadas en el CEMET, terminando la ejecución del proyecto probablemente en menos de dos años. El cuello de botella que se percibe es el acceso al instrumento conseguido por este equipo de trabajo como donación al CEMET, pero esa dificultad podría soslayarse retomando el primitivo convenio de palabra con el director del laboratorio del CeNARD (y actual profesor de la UNAJ), donde las muestras de plasma podrían ser procesadas y analizadas con un instrumento de GC-MS con tecnología de cuadrupolo, o eventualmente con el instrumento de trampa de iones.
Por otra parte, de poder acceder al instrumento de LC-MS del CEMET se estaría en condiciones de continuar la colaboración con la Dra. Chiaramoni de la UNQ en apoyo de la búsqueda de condiciones óptimas de preparación del péptido sintético conjugado.
Conclusiones
Del análisis de los resultados obtenidos puede concluirse que este grupo de investigación ha realizado gran parte de las tareas de puesta a punto de las técnicas de preparación y procesamiento de las muestras (una tarea de mayor dificultad que el procesamiento de las muestras en sí mismo) para el análisis cualicuantitativo de ácidos grasos totales, los ligados a lípidos complejos y los libres en circulación, en muestras de plasma de pacientes diagnosticados con HPA y de muestras de plasma del correspondiente grupo control. Los detalles del procedimiento analítico desarrollado, los cromatogramas y los espectros de masa obtenidos así lo confirman. Es de destacar que, una semana antes del comienzo de la cuarentena del 2020, se había comenzado a procesar las muestras recolectadas por el sector de Neumonología, gracias al trabajo conjunto con el doctor Daniel Aimone, tareas que quedaron truncas. Sin embargo, confiamos que estas puedan retomarse con el apoyo que siempre nos proporcionaron la Universidad Nacional Arturo Jauretche (UNAJ) y, eventualmente, el CeNARD.
Referencias
- Björkhem, I., Miettinen, T., Reihnér, E., Ewerth, S., Angelin, B. y Einarsson, K. (1987). Correlation between serum levels of some cholesterol precursors and activity of HMGCoA reductase in human liver. Journal of Lipid Research, 28, pp. 1137-1143.
- Boden, G. (2006). Fatty acid-induced inflammation and insulin resistance in skeletal muscle and liver. Current Diabetes Report, 6, pp. 177-181.
- Caballero, G. M., Padin, E. V. y Pollio, M. L. (2014). Chemical Composition of Oleoresins from Berries of Schinus Molle L. Grown in Buenos Aires Province (Argentina). Journal of Food Technology, 12(3), pp. 73-77.
- Faccone, D., Veliz, O., Corso, A., Noguera, M., Martínez, M., Payes, C., Semorile, L. y Maffía, P. C. (2014). Antimicrobial activity of de novo designed cationic peptides against multi-resistant clinical isolates. European Journal of Medicinal Chemistry, 71(7), pp. 31-35.
- Garg, U. y Hammett-Stabler, C. A. (Eds.). (2010). Clinical Applications of Mass Spectrometry: Methods and Protocols (pp. 1-7). Methods in Molecular Biology, 603. Humana Press.
- Geoghegan, K. F. y Stroh, J. G. (1992). Site-directed conjugation of nonpeptide groups to peptides and proteins via periodate oxidation of a 2-amino alcohol. Application to modification at N-terminal serine. Bioconjugate Chemistry, 3(2), pp. 138-146.
- Jones, P. M. y Bennett, M. J. (2010). Urine Organic Acid Analysis for Inherited Metabolic Disease Using Gas Chromatography-Mass Spectrometry. En U. Garg y C. A. Hammett-Stabler (Eds.). Clinical Applications of Mass Spectrometry (pp. 423-432). Humana Press.
- Lepage, G. y Roy, C. (1988). Specific methylation of plasma nonesterified fatty acids in a one-step reaction. Journal of Lipid Research, 29, pp. 227-235.
- Padin, E. V. (2015). Obtención, caracterización y determinación de la actividad antimicrobiana de la oleorresina de las bayas de Aguaribay (Schinus molle L.) (Tesis doctoral). Universidad Nacional de Quilmes. Quilmes.
- Padin, E. V., Caballero, G. M. y Pollio, M. L. (2015). Study of the Antimicrobial Properties of Oleoresins from Berries of Aguaribay (Schinus molle L.) on Fungi and Food Spoilage Yeasts. Journal of Food Technology, 13(3), pp. 18-24.
- Pasquali, M. y Sawyer, B. (2008). Newborn Screening. En C. Burtis, E. Ashwood, D. Bruns y B. Sawyer (Eds.). Tietz Fundamentals of Clinical Chemistry, pp. 825-835. Missouri: Saunders Elsevier.
- Quehenberger, O., Armando, A., Brown, A., Milne, S., Myers, D., Merrill, A., Bandyopadhyay, S., Jones, K., Kelly, S., Shaner, R., Sullards, C., Wang, E., Murphy, R., Barkley, R., Leiker, T., Raetz, C., Guan, Z., Laird, G., Six, D.… (2010). Lipidomics reveals a remarkable diversity of lipids in human plasma. Journal of Lipid Research, 51, pp. 3299-3305.
- Riccardi, G., Giacco, R. y Rivellese, A. A. (2004). Dietary fat, insulin sensitivity and the metabolic syndrome. Clinical Nutrition, 23, pp. 447-56.
- Rodríguez-Ruiz, J., Belarbi, E., García Sánchez, J. L. y López Alonso, D. (1998). Rapid simultaneous lipid extraction and transesterification for fatty acid analyses. Biotechnology Techniques, 1(9), pp. 689-691.
- Ross, D. J., Hough, G., Hama, S., Aboulhosn, J., Belperio, J. A., Saggar, R. y Van Lenten, B. J., Ardehali, A., Eghbali, M., Reddy, S., Fogelman, A. y Navab, M. (2015). Proinflammatory high-density lipoprotein results from oxidized lipid mediators in the pathogenesis of both idiopathic and associated types of pulmonary arterial hypertension. Pulmonary Circulation, 5(4), pp. 640-648.
- Sookoian, S. y Pirola, C. J. (2008). Non-alcoholic fatty liver disease is strongly associated with carotid atherosclerosis: a systematic review. Journal of Hepatology, 49, pp. 600-607.
- —– (2012). DNA methylation and hepatic insulin resistance and steatosis. Current Opinion in Clinical Nutrition & Metabolic Care, 15, pp. 350-356.
- Talati, M. y Hemnes, A. (2015). Fatty acid metabolism in pulmonary arterial hypertension: role in right ventricular dysfunction and hypertrophy. Pulmonary Circulation, 5, pp. 269-278.
Notas:
[1] Estos ácidos grasos de número impar de átomos de carbono no se encuentran en el organismo, por ello son compuestos aptos para su uso como estándares internos. Asimismo, usamos dos en particular, ya que estos eluyen en diferentes regiones del cromatograma, permitiendo así una cuantificación relativa más precisa de los correspondientes ácidos grasos endógenos que eluyen en tiempos cercanos a cada uno de estos estándares.
